翰宇藥業(yè)再次“零缺陷”通過(guò)美國(guó)FDA現(xiàn)場(chǎng)核查

翰宇藥業(yè)全資子公司翰宇藥業(yè)(武漢)順利完成了為期5天的美國(guó)FDA現(xiàn)場(chǎng)核查,F(xiàn)DA按照cGMP標(biāo)準(zhǔn)(現(xiàn)行藥品生產(chǎn)質(zhì)量管理規(guī)范)對(duì)翰宇藥業(yè)原料藥生產(chǎn)系統(tǒng)、設(shè)備設(shè)施系統(tǒng)、物料系統(tǒng)、質(zhì)量控制系統(tǒng)、包裝貼簽系統(tǒng)以及質(zhì)量系統(tǒng)的現(xiàn)場(chǎng)及各類體系文件進(jìn)行了嚴(yán)苛、全面、細(xì)致的查驗(yàn),并于11月29日下午,給予了“零缺陷”結(jié)論,即未收到任何483表(不符合項(xiàng))!
此次順利通過(guò)FDA檢查,標(biāo)志著翰宇藥業(yè)繼2023年龍華總部研發(fā)中心“零缺陷”通過(guò)FDA檢查之后,再次取得這一重要成果。這不僅再次驗(yàn)證了翰宇藥業(yè)在質(zhì)量管理方面的國(guó)際領(lǐng)先水平,也標(biāo)志著公司在國(guó)際化進(jìn)程中的步伐更加穩(wěn)健,邁向更高的發(fā)展目標(biāo)。
FDA(美國(guó)食品藥品監(jiān)督管理局)是由美國(guó)聯(lián)邦政府授權(quán),負(fù)責(zé)監(jiān)管食品、藥品、化妝品和醫(yī)療器械等產(chǎn)品質(zhì)量與安全的國(guó)家機(jī)構(gòu)。通過(guò)FDA的檢查,意味著產(chǎn)品符合全球高標(biāo)準(zhǔn),被公認(rèn)為有效且安全,具有全球市場(chǎng)的認(rèn)可度。
翰宇藥業(yè)始終秉持質(zhì)量至上的發(fā)展理念,旗下坪山制劑生產(chǎn)基地、武漢原料藥生產(chǎn)基地、龍華總部研發(fā)中心等均已通過(guò)FDA cGMP標(biāo)準(zhǔn)現(xiàn)場(chǎng)檢查,且多次通過(guò)歐盟、韓國(guó)、巴西等國(guó)家和地區(qū)的GMP認(rèn)證。這為公司利拉魯肽上市銷售以及未來(lái)其他產(chǎn)品的國(guó)際化奠定了堅(jiān)實(shí)基礎(chǔ)。
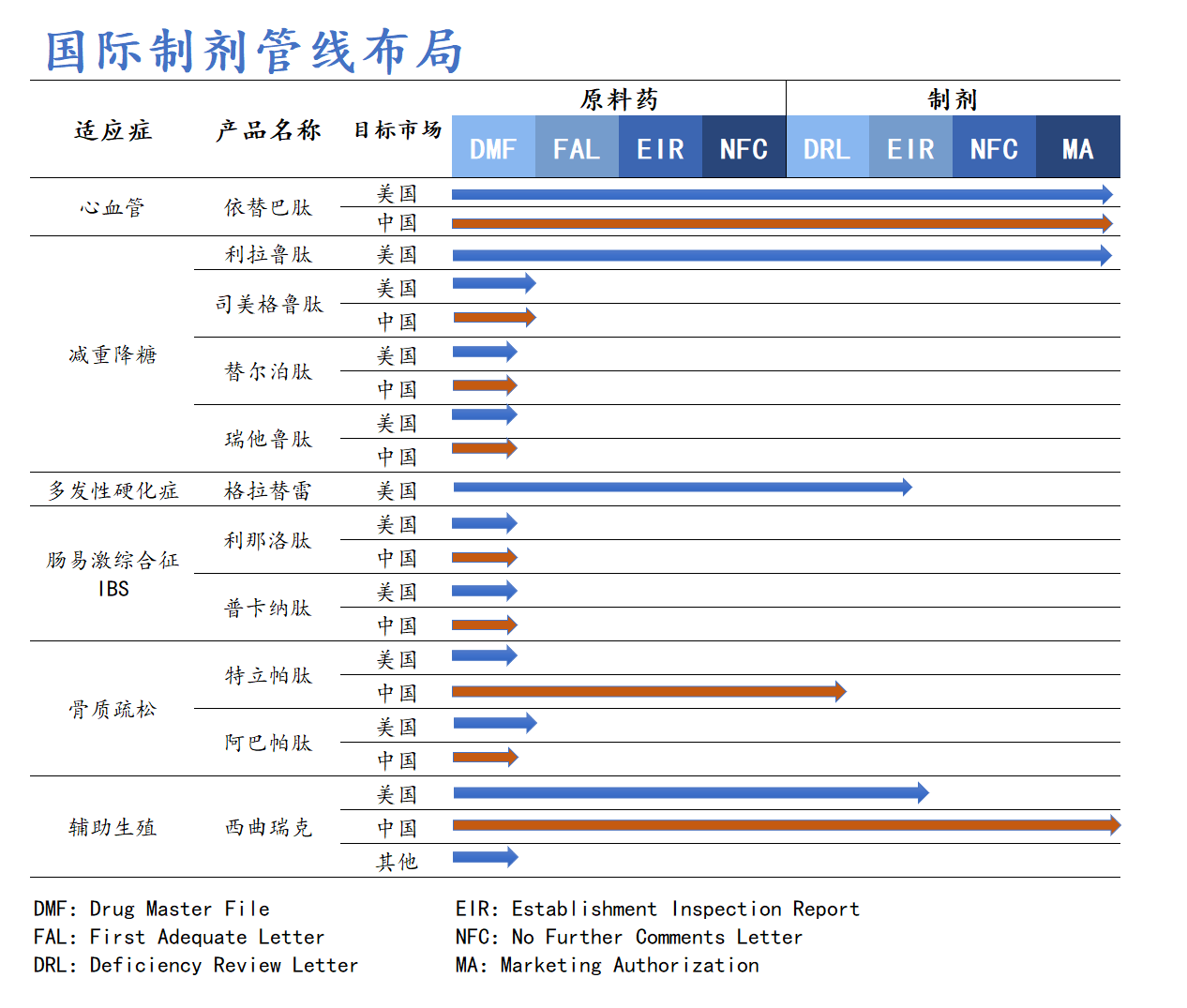
國(guó)際制劑管線方面,作為多肽行業(yè)的先進(jìn)企業(yè),翰宇藥業(yè)堅(jiān)持技術(shù)創(chuàng)新,不斷拓展產(chǎn)品管線布局,積極尋找優(yōu)勢(shì)互補(bǔ)、資源共享的優(yōu)質(zhì)國(guó)際合作伙伴,國(guó)際管線布局涵蓋利拉魯肽、司美格魯肽、替爾泊肽、瑞他魯肽、格拉替雷等重磅產(chǎn)品。其中利拉魯肽已于9月23日向FDA發(fā)起上市銷售申請(qǐng)且獲美國(guó)FDA受理,目標(biāo)審評(píng)日期為2024年12月23日。
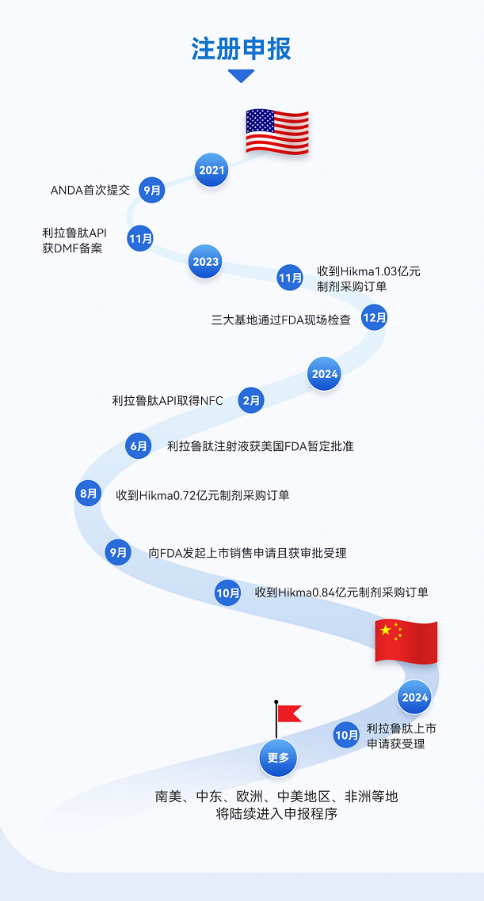
此外,多肽原料藥方面,翰宇藥業(yè)能夠?qū)崿F(xiàn)幾乎所有已上市多肽藥物原料藥的開(kāi)發(fā)和生產(chǎn),并對(duì)長(zhǎng)鏈多肽原料藥(氨基酸數(shù)量在30個(gè)以上)的開(kāi)發(fā)具有獨(dú)到的技術(shù)優(yōu)勢(shì)。目前,公司已有30多個(gè)多肽原料藥取得《藥品生產(chǎn)許可證》,為滿足海外市場(chǎng)增量需求,翰宇藥業(yè)武漢原料藥生產(chǎn)基地產(chǎn)能可達(dá)噸級(jí)。
未來(lái),翰宇藥業(yè)將繼續(xù)發(fā)揮FDA認(rèn)證帶來(lái)的質(zhì)量?jī)?yōu)勢(shì),不斷增強(qiáng)綜合競(jìng)爭(zhēng)力,為公司的高質(zhì)量發(fā)展和提升國(guó)際市場(chǎng)品牌影響力打下更加堅(jiān)實(shí)的基礎(chǔ)!